Меню
Найти врача
тестостерон и андрогенный дефицит: диагностика и современные подходы к лечению
Тестостерон, основной мужской половой гормон, играет ключевую роль в поддержании физического, сексуального и психоэмоционального здоровья мужчины. Он отвечает за развитие вторичных половых признаков, регуляцию либидо, эректильной функции, плотности костной ткани, мышечной массы и настроения. Снижение уровня тестостерона, известное как андрогенный дефицит или гипогонадизм, является распространенной проблемой, которая значительно ухудшает качество жизни мужчин и может быть индикатором серьезных системных нарушений в организме[1].
В России, по данным ретроспективного одноцентрового исследования, проведенного в 2021 году (Павлова З.Ш. и соавт.), распространенность дефицита общего тестостерона среди мужчин, обращавшихся к врачу-эндокринологу, составила 57,5%[2]. В этом исследовании была проанализирована 301 история болезни пациентов, и дефицит тестостерона определялся как уровень < 12,1 нмоль/л при наличии трех симптомов, соотносимых с андрогенным дефицитом. Методология включала статистическую обработку данных с использованием IBM SPSS Statistics 23.0, дисперсионный анализ (ANOVA) или критерий Краскела — Уоллиса для проверки гипотезы о равенстве средних значений, и коэффициент Спирмена для оценки корреляции. Эти данные подчеркивают актуальность проблемы и необходимость своевременной диагностики и коррекции.
Глобальная распространенность дефицита тестостерона (ДТ) варьируется от 10% до 40%[5]. Важно различать биохимический гипогонадизм (низкий уровень тестостерона в крови) и симптоматический гипогонадизм (низкий уровень тестостерона в сочетании с характерными клиническими проявлениями). Диагностика ДТ является предметом дискуссий, поскольку используются различные пороговые значения общего тестостерона (200–400 нг/дл), и врачи по-разному оценивают значимость клинических симптомов. Существуют также значительные глобальные различия в схемах назначения тестостерон-заместительной терапии (ТЗТ)[6].
Например, в США распространенность биохимического ДТ среди мужчин среднего и пожилого возраста (24–39%) значительно выше, чем в других частях мира[6]. Однако, если учитывать не только биохимические показатели, но и наличие трех и более симптомов гипогонадизма, то распространенность симптоматического гипогонадизма снижается до 6% (уровень доказательности: Систематический обзор)[6]. В Европе распространенность диагностированного биохимического гипогонадизма ниже, чем в США, и составляет 8–20%, а при учете симптомов симптоматический гипогонадизм снижается до 10–12%[6]. Аналогичные тенденции наблюдаются в Азии и Южной Америке, где распространенность биохимического гипогонадизма составляет 17–33%, но при наличии соответствующих симптомов снижается вдвое[6]. Эти данные подчеркивают важность комплексного подхода к диагностике, учитывающего как лабораторные показатели, так и клиническую картину.
Эти исследования демонстрируют, что дизайн исследования (биохимический скрининг vs. симптоматический скрининг) и возрастные группы значительно влияют на оцениваемую распространенность дефицита тестостерона.
С возрастом уровень тестостерона у мужчин постепенно снижается, после 30-35 лет со скоростью около 1-2% в год[4]. Этот процесс получил название мужского климакса или андропаузы (частичный возрастной дефицит андрогенов, PADAM). В отличие от женского климакса, андропауза развивается более плавно и не всегда сопровождается выраженными симптомами. Однако у многих мужчин это состояние приводит к значительному ухудшению самочувствия.
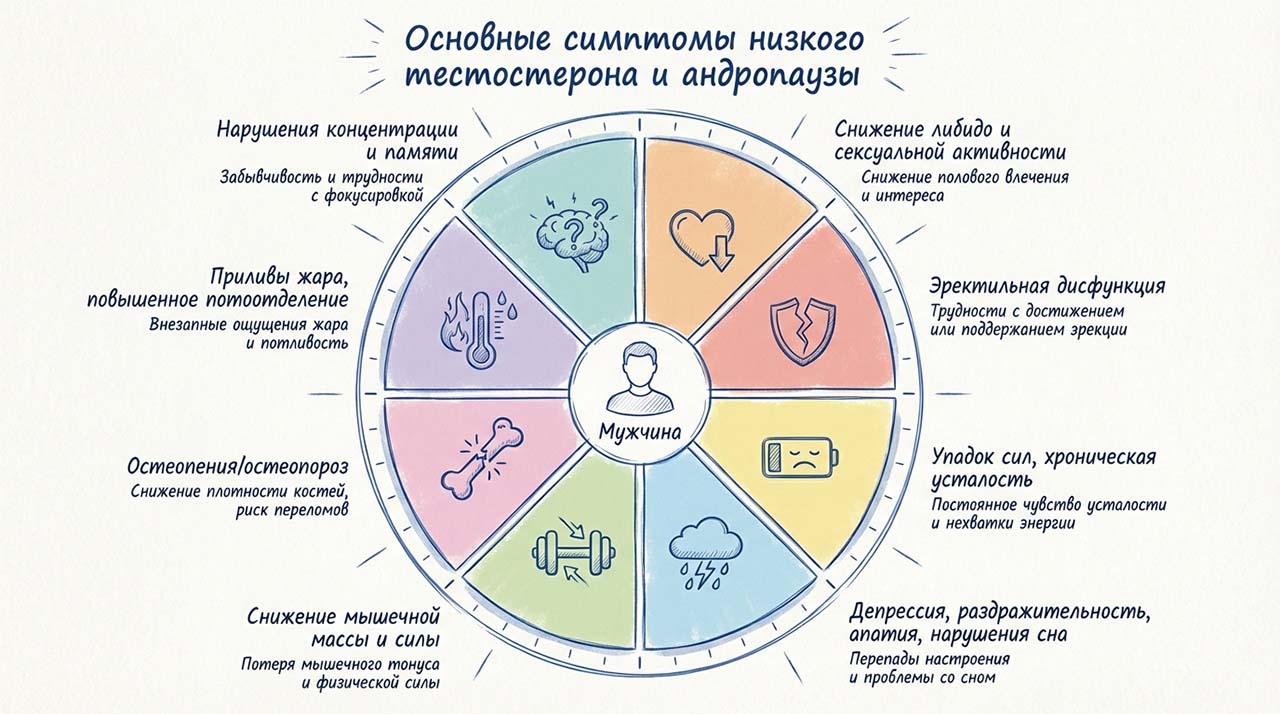
Для скрининга и оценки выраженности симптомов андрогенного дефицита используются специализированные опросники, такие как AMS (Aging Males’ Symptoms scale) и ADAM (Androgen Deficiency in the Aging Male). Однако важно учитывать их ограничения и интерпретировать результаты в контексте клинической картины и лабораторных данных[11, 12].
Опросник AMS является самозаполняемой шкалой, разработанной для оценки симптомов старения у мужчин, их динамики с течением времени и эффективности терапии. Он широко используется во всем мире и переведен на множество языков. Опросник включает вопросы, касающиеся психологических, соматических и сексуальных симптомов. Надежность и валидность шкалы AMS подтверждены многочисленными исследованиями[9].

Недавние исследования (2025 г.) показывают, что баллы по шкале AMS могут слабо коррелировать с уровнем тестостерона у мужчин с сопутствующими заболеваниями, такими как сахарный диабет 2 типа. Диабетические осложнения могут самостоятельно повышать баллы AMS, что требует осторожности и, возможно, использования более высоких пороговых значений при скрининге гипогонадизма в этой популяции[14].
Опросник ADAM (Androgen Deficiency in the Aging Male), разработанный Morley и соавт., состоит из 10 вопросов с ответами «да» или «нет», направленных на выявление ключевых симптомов андрогенного дефицита[10].
Важно отметить, что опросники являются скрининговыми инструментами и не могут служить единственным основанием для постановки диагноза. Они помогают выявить мужчин, нуждающихся в дальнейшем обследовании, включая лабораторное определение уровня тестостерона. Для повышения точности диагностики рекомендуется сочетать данные опросников с биохимическими показателями и учитывать индивидуальные особенности пациента.
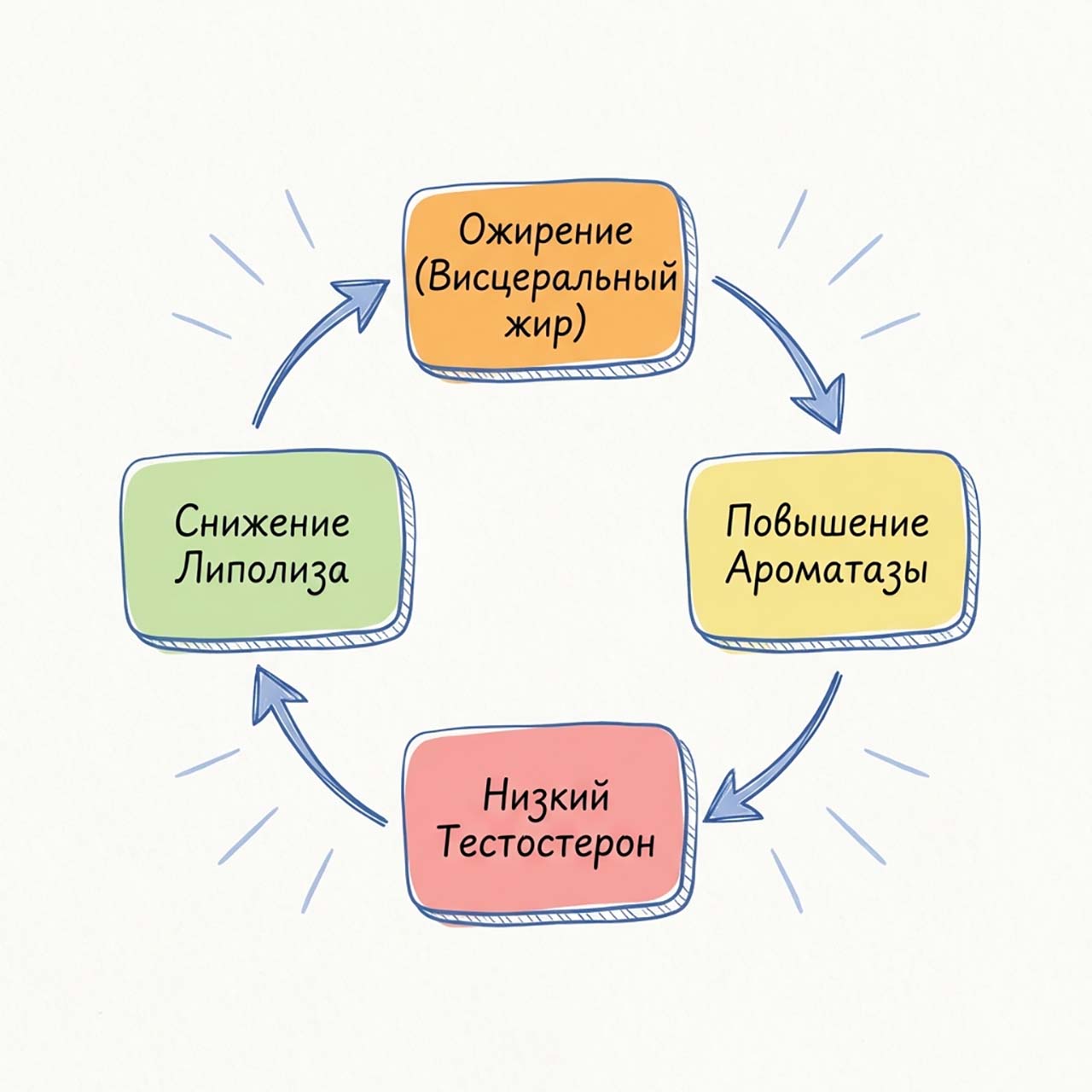
Андрогенный дефицит часто не является изолированной проблемой, а тесно связан с другими метаболическими нарушениями, усугубляющими возрастное снижение тестостерона. Одним из наиболее ярких примеров является взаимосвязь между низким тестостероном и ожирением, особенно висцеральным. Жировая ткань, особенно абдоминальная, содержит фермент ароматазу, который превращает тестостерон в эстрогены. Повышение уровня эстрогенов, в свою очередь, подавляет выработку тестостерона гипофизом, создавая «порочный круг»[6]. Этот механизм особенно актуален в контексте возрастного гипогонадизма, где снижение уровня тестостерона может быть как причиной, так и следствием развития метаболических нарушений, таких как инсулинорезистентность и сахарный диабет 2 типа (уровень доказательности: Систематический обзор, Мета-анализ).
Кроме того, дефицит тестостерона ассоциируется с повышенным риском развития сахарного диабета 2 типа, метаболического синдрома, сердечно-сосудистых заболеваний и остеопороза. Поэтому комплексный подход к диагностике и лечению андрогенного дефицита крайне важен.
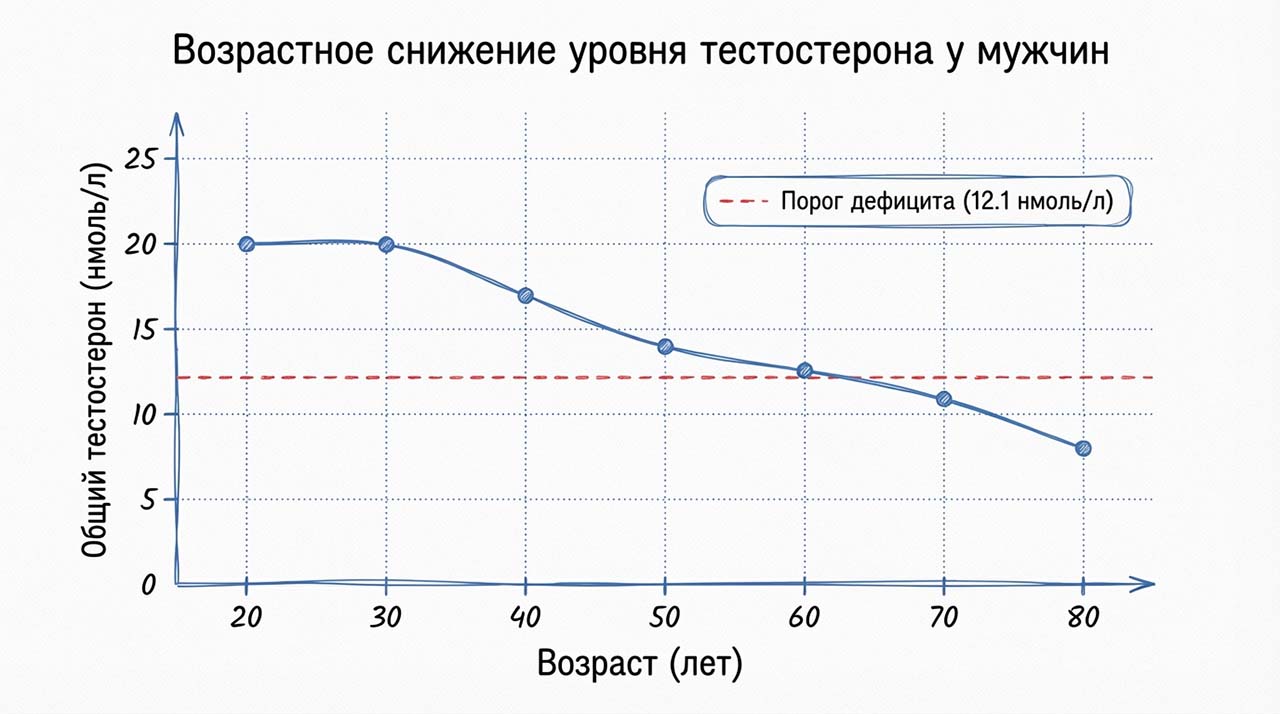
Согласно актуальным клиническим рекомендациям Минздрава РФ, в частности документу «Синдром гипогонадизма у мужчин» (2021-2023 гг.), диагностика гипогонадизма должна основываться на сочетании клинических симптомов и лабораторного подтверждения низкого уровня тестостерона. Пороговым значением для общего тестостерона считается менее 12.1 нмоль/л (или 350 нг/дл)[1].
Важно: Тестостерон-заместительная терапия (ТЗТ) назначается только при наличии как клинических симптомов, так и лабораторно подтвержденного дефицита тестостерона. Перед началом ТЗТ необходимо исключить противопоказания и провести тщательное обследование пациента.
Современные подходы к лечению андрогенного дефицита включают не только ТЗТ, но и коррекцию образа жизни: нормализацию веса, регулярные физические нагрузки, отказ от вредных привычек, а также психотерапевтическую поддержку при необходимости[4].
Согласно рекомендациям Американской Урологической Ассоциации (AUA) 2024 года и последним обзорам 2025 года, ТЗТ должна быть направлена на достижение уровня общего тестостерона в средней трети нормального референсного диапазона (обычно 450-600 нг/дл)[6, 13]. Современная медицина предлагает широкий спектр лекарственных форм, каждая из которых имеет свои особенности фармакокинетики и профиль безопасности.
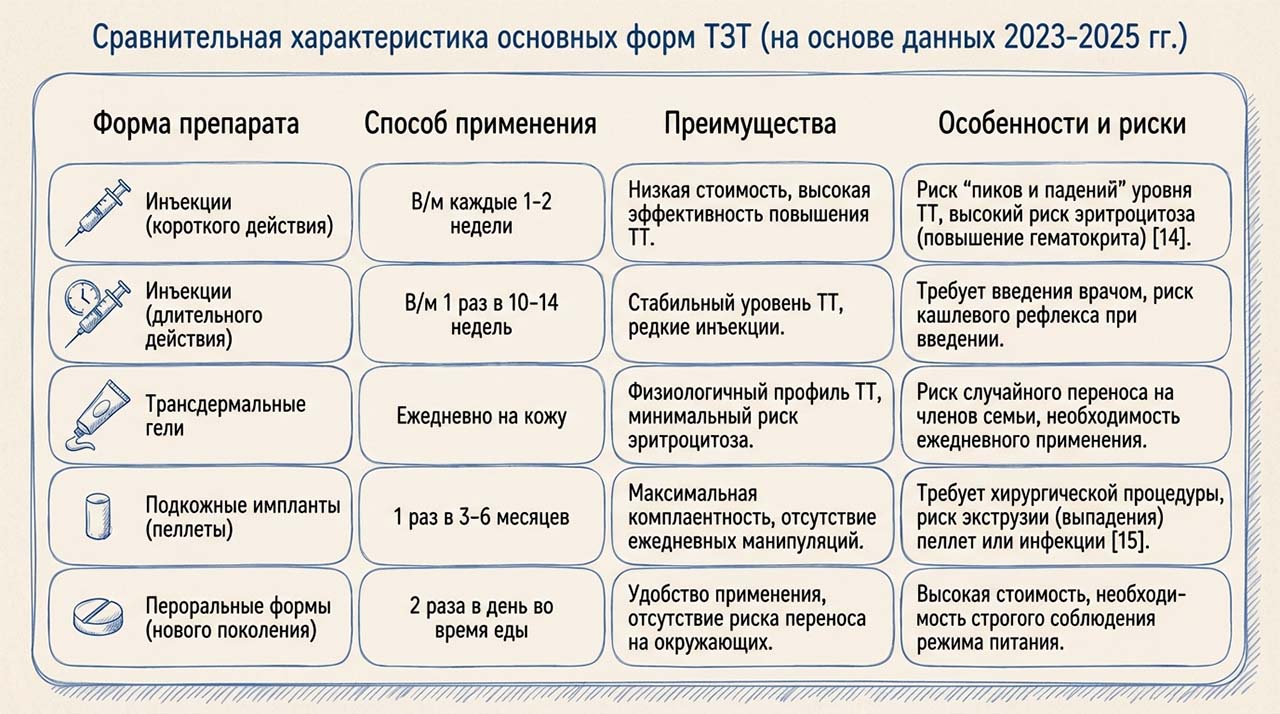
Систематические обзоры подтверждают, что ТЗТ не только эффективно восстанавливает уровень тестостерона, но и значимо улучшает качество жизни, показатели минеральной плотности костей и липидный профиль (уровень доказательности: Мета-анализ, 2024)[13, 14]. Важнейшим событием стало завершение исследования TRAVERSE (2023-2024), которое на выборке более 5000 мужчин доказало отсутствие повышения риска серьезных сердечно-сосудистых событий (MACE) при правильно назначенной ТЗТ у пациентов с гипогонадизмом (уровень доказательности: Рандомизированное контролируемое исследование). Более того, мета-анализ 2025 года указывает на потенциальное улучшение эректильной функции даже у пациентов, ранее не отвечавших на терапию ингибиторами ФДЭ-5 (уровень доказательности: Мета-анализ)[14].
Перед началом ТЗТ и в процессе лечения необходим тщательный мониторинг уровня тестостерона, гематокрита, ПСА и общего состояния пациента[6].
Для получения более подробной информации о современных подходах к диагностике и лечению урологических заболеваний, а также о доступных решениях, вы можете ознакомиться с разделом «Решения для пациентов» на нашем сайте.